Services on Demand
article
Indicators
Share
Journal of Human Growth and Development
Print version ISSN 0104-1282On-line version ISSN 2175-3598
J. Hum. Growth Dev. vol.28 no.1 São Paulo Jan./Mar. 2018
http://dx.doi.org/10.7322/jhgd.143846
ARTIGO ORIGINAL
Recém-nascidos com sepse por Estafilococos aureus e coagulasa-negativo tratados com Vancomicina, após aumento do nível sérico no vale
Rosane OkasakiI; Werther Brunow de CarvalhoII; Maria Esther Jurfest Rivero CecconIII
IEstudante
de graduação. Programa de Iniciação Científica.
Faculdade de Medicina da Universidade de São Paulo
IIProfessor Titular Terapia Intensiva- Neonatologia do Instituto
da Criança- Hospital das Clínicas da Faculdade de Medicina da
Universidade de São Paulo. Graduado em Medicina, Faculdade de Ciências
Médicas de Santos (1977), Título de Especialista em Terapia Intensiva
e Neonatologia, em Nutrição Parenteral e Enteral. Atualmente é
Chefe da UTI Hospital Santa Catarina
IIILivre Docente. Chefe da UTI neonatal do Instituto da Criança.
Coordenadora de Ensino da Disciplina de Neonatologia e de Pesquisa da UTI Neonatal
RESUMO
INTRODUÇÃO:
A Vancomicina é um antibiótico glicopeptídico considerado
padrão-ouro no tratamento de infecções por estafilococos
resistentes à oxacilina.
OBJETIVO: Analisar a concentração do nível sérico
no vale (uma hora antes da próxima administração da dose
do medicamento) de Vancomicina em recém-nascidos com infecção
por Staphylococcus aureus ou coagulase- negativa resistente à Oxacilina.
MÉTODO: Trata-se de estudo experimental e com coleta de dados
entre os anos de 2001 e 2016. Foram selecionados randomicamente 30 pacientes
que tinham como diagnóstico sepse por Staphylococcus aureus e coagulase-negativa
e fizeram uso da Vancomicina como forma de tratamento e tiveram seus níveis
séricos coletados e registrados nos prontuários.
RESULTADOS: Dos 30 pacientes incluídos no presente estudo, 80%
eram pré-termos. Dentre todos os recém-nascidos as médias
das concentrações séricas no vale da Vancomicina foram
de 40% adequadas, 13,34% abaixo do esperado e 46,67% acima dos valores de referência.
Em 7 µpacientes (23,34%) o primeiro nível sérico no vale
da Vancomicina coletado foram adequados, porém em 9 (30%) e 14 (46,67%)
a concentração sérica no vale foi, respectivamente, abaixo
e acima dos valores corretos. Após a mudança de dose daqueles
que não obtiveram níveis adequados, apenas 3 dos 14 pacientes
em que a primeira dose não fora adequada tiveram uma média de
nível sérico total dentro do esperado, enquanto os 11 restantes
permaneceram com níveis elevados, os quais causam grandes preocupações
devido ao fato de além de não estar sendo tratada a infecção,
o nível sérico elevado acarreta em problemas nefrotóxicos
e ototóxicos. O monitoramento dos níveis séricos no vale
da Vancomicina é de grande importância, pois minimiza os efeitos
nefrotóxicos, assim aumentando a eficácia do medicamento. O ajuste
posológico da Vancomicina em pacientes em estado grave internados em
uma Unidade de Terapia Intensiva é importante e necessita de mais estudos
referentes à essa área, assim como o trabalho de um corpo multidisciplinar
torna o tratamento melhor e mais específico.
CONCLUSÃO: As concentrações dos níveis séricos
no vale de Vancomicina em pacientes internados em Unidade de cuidados intensivos
neonatais de Hospital de Referencia da América Latina entre 10 e 15 µg/mL
para serem bactericidas no entanto não é o que observamos nesta
pesquisa.
Palavras-chave: vancomicina, monitorização terapêutica, níveis séricos no vale, unidade de terapia intensiva neonatal, recém-nascidos, Staphylococcus aureus.
INTRODUÇÃO
A infecção por estafilococos tanto aureus como Coagulasse-negativa é a mais comum em unidades de terapia intensiva tanto neonatal quanto pediátrica1,2, e tem impacto significativo na mortalidade e morbidade dos pacientes3,4,5. A partir da década de 80 surgiram os estafilococos resistentes à penicilina e atualmente ambos os tipos são sensíveis apenas a Vancomicina. Por este fato, este medicamento é considerado há muito tempo o padrão-ouro na terapia contra estes agentes infecciosos6.
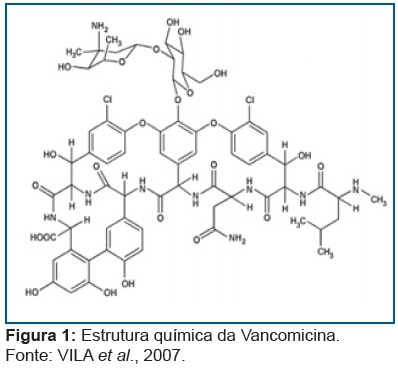
A Vancomicina foi aprovada para uso nos Estados Unidos pela Food and Drug Administration (FDA) em 1958 para tratar a infecção por Staphylococcus aureus resistente à penicilina1. Ela é um antibiótico glicopeptídico com estrutura complexa, contém aminoácidos e açúcares e possui alto peso molecular com atividade variável na faixa de pH entre 6,0 e 8,02,3.
Quando se administra a Vancomicina são várias as situações que requerem a monitorização dos seus níveis séricos e o ajuste posológico das doses administradas. Fatores clínicos como o local e a gravidade da infecção, o agente infeccioso suspeitado ou confirmado, a doença de base e terapias concomitantes7, e o fato de este fármaco apresentar uma estreita margem terapêutica, aumenta o risco de efeitos colaterais tais como a nefro e o ototoxicidade; reações de pele como eritema, "flushing histamina like", além de outras reações anafiláticas quando se administra anestésicos. A associação com aminoglicosídeos e furosemida que é frequente no paciente com sepse, aumenta a toxicidade. Os efeitos no bloqueio neuromuscular podem estar aumentados quando relaxantes musculares não despolarizantes são administrados.
Existem importantes variações farmacocinéticas interindividuais (idade, peso, função renal), que realçam a importância da monitorização e do ajuste posológico do medicamento na prática clínica8. Porém, mesmo sendo um fármaco utilizado há mais de meio século nos cuidados neonatais, as buscas pela dosagem e eficácia corretas ainda nos dias de hoje demonstram sua complexidade farmacológica.
Os prematuros, por apresentarem concentração sérica de proteínas diminuída, alta concentração de albumina fetal, a qual possui afinidade diminuída para ligação às drogas, pH plasmático baixo, o que reduz a ligação proteica às drogas ácidas, e concentração sérica de moléculas competidoras à ligação das drogas com as proteínas, como a bilirrubina e os ácidos graxos livres, são susceptíveis a maior concentração de droga livre e biodisponível. Assim, uma dose padrão se torna uma dose exagerada e causa efeitos tóxicos. Por outro lado, o maior volume de distribuição de drogas aos tecidos acarreta maior necessidade de concentração de drogas por quilo de peso corporal para manter a concentração sérica adequada, pois as drogas livres de proteínas estão, também, mais disponíveis para serem metabolizadas e excretadas9.
Os valores terapêuticos para o uso de Vancomicina de acordo com o Neofax® (livro de doses utilizados na maioria das Unidades Neonatais) até 2009 eram de 5-10 µg/ml para concentrações no vale (4 a 8 vezes MIC) e 20-40 µg/ml para concentrações no pico (10 a 30 MIC) com doses de 10-15 mg/kg/dose10. Atualmente, as referências neonatais recomendam concentrações séricas no vale mais elevadas de 10-15 µg/ml, contudo as doses permaneceram inalteradas11,12.
Assim, o objetivo é analisar a concentração dos níveis séricos no vale (uma hora antes da próxima administração da dose do medicamento) de Vancomicina em recém-nascidos admitidos em uma unidade de terapia intensiva neonatal com infecção de corrente sanguínea por Staphylococcus aureus ou coagulase-negativas resistentes a oxacilina estão adequadas e de acordo com a literatura.
MÉTODO
Trata-se de um estudo retrospectivo descritivo e de intervenção, quando os níveis do medicamento encontravam-se fora da faixa da normalidade, realizado no Centro de Tratamento Intensivo Neonatal (CTNI-2) do Instituto da Criança do Hospital das Clínicas da Universidade de São Paulo, o qual conta com 20 leitos que recebem para internação recém-nascidos em estado grave tanto com doenças clínicas quanto cirúrgicas, que necessitam de cuidados especializados e por 24 horas.
Define-se vale ao período de tempo de uma hora antes da próxima administração da dose do medicamento. A escolha do vale se deu em virtude de ser rotineiramente dosado para indicar os níveis/valores da dosagem adequada do fármaco na condução terapêutica do recém-nascido até o final da ação medicamentosa.
Critérios de inclusão
Foi disponibilizada uma lista de pacientes que, segundo o levantamento do registro da Unidade e do Hospital, foram internados na UTI neonatal do Instituto da Criança e possuíam o diagnóstico de sepse por Staphylococcus aureus e/ou coagulase-negativa.
A partir desta lista, proveu-se a randomização dos recém-nascidos que foram internados entre os anos de 2001 e 2016 e com idade menor que um ano de vida.
Desse modo, incluíram-se os dados registrados nos prontuários de pacientes com infecção da corrente sanguínea por Staphylococcus aureus e coagulase-negativa que utilizaram a Vancomicina como forma de tratamento e tiveram o nível sérico coletado e registrado. Levantaram-se também dados como peso, idade, idade gestacional e as doses administradas da Vancomicina junto do intervalo de tempo da administração da mesma.
Critérios de exclusão
Foram excluídos os pacientes cujos dados registrados nos prontuários não apresentavam registro do nível sérico no vale de Vancomicina ou não a receberam como forma de tratamento.
Foram englobados todos os pacientes que obtiveram níveis séricos no vale de Vancomicina abaixo, adequado ou acima dos valores de referência, mesmo que o período de admissão destes pacientes possuía níveis séricos de referência distintos.
A prescrição da Vancomicina foi feita de acordo com a literatura seguida, o Neofax®, o qual sugere doses de acordo com o peso e idade gestacional do recém-nascido. As doses sugeridas são de 10-15 mg/kg/dose com intervalos de administração seguidos empiricamente, assim, poderiam ser de 6/6 horas, 8/8 horas, 12/12 horas, 18/18 horas até 24/24 horas dependendo do resultado da coleta do nível sérico no vale da Vancomicina, ou seja, este estando acima ou abaixo do valor de referência de 10-15 µg/ml, modificava-se o intervalo de tempo da administração do medicamento.
O vale da Vancomicina como citado na introdução é uma hora antes da próxima administração do medicamento e representa a eficácia do mesmo, que deve-se encontrar ainda entre os valores desejados, ou seja este ainda estaria agindo mesmo no final do horário, antes da próxima dose.
Os dados coletados dos níveis séricos foram analisados estatisticamente através de médias, medianas, desvios padrão e % de desvio da média.
O presente estudo foi aprovado pela Comissão de Pesquisa e Ética do Departamento de Pediatria da Faculdade de Medicina da Universidade de São Paulo, número do protocolo : 1.684976)
RESULTADOS
Foram incluídos 30 recém-nascidos, sendo que 24 (80%) prematuros; treze do sexo feminino (43,4%). A média de idade em que fora iniciado o tratamento com Vancomicina foi de 21,94 dias de vida. Através dos registros de exames laboratoriais realizados, obteve-se hemocultura positiva para Staphylococcus aureus em 12 pacientes e hemocultura positiva para S. coagulase-negativa 18 recém-nascidos (tabela 1 e tabela 2).
Dos 30 recém-nascidos, 12 (40%) obtiveram média adequada de níveis séricos, porém quatro (13,34%) tiveram a média abaixo do esperado e 14 (46,67) com média acima dos valores de referência (tabela 3).
Após 72 horas, os 30 recém-nascidos estudados tiveram o nível sérico no vale de Vancomicina reavaliados. Dentre eles, sete (23,34%), nove (30%) e 14 (46,67) tiveram, respectivamente, um nível sérico adequado, abaixo e acima dos referenciais de literatura. Com isso, houve a mudança na dose e/ou no intervalo de administração da dose prescrita para os recém-nascidos que obtiveram níveis séricos abaixo e acima do esperado, coletando um segundo nível sérico após três dias. Pode-se constatar que daqueles que tiveram o primeiro nível sérico no vale de Vancomicina adequado (23,34%) e abaixo (30%) da referência, em ambos os casos 13,24% dos pacientes obtiveram a média total de seus níveis séricos coletados adequados havendo ajuste correto da dose.
Porém, os 14 pacientes que tiveram um resultado elevado na primeira coleta de nível sérico no vale e tiveram suas doses de Vancomicina modificadas, observou-se que a média de todos os níveis séricos de 11 destes pacientes (36,67%) permaneceram elevadas e apenas três (10%) foram adequadas.
Apenas 11 pacientes (36,67%) dispunham do primeiro nível sérico no vale de Vancomicina registrado. Dentre eles, três (10%) estavam abaixo dos valores de referência e quatro (13,34%) estavam com níveis adequados assim como a mesma quantidade de pacientes estavam com os níveis elevados (gráfico 1).
DISCUSSÃO
A análise dos níveis séricos no vale de Vancomicina realizada no presente estudo mostrou que 60% dos pacientes se encontravam fora dos alvos propostos, sendo que destes, 13,64% estavam abaixo do esperado e 46,36% encontravam-se acima dos valores de referência. Níveis séricos abaixo dos níveis terapêuticos causam grande preocupação, pois há a demora do tratamento da infecção assim como maior suscetibilidade à resistência da bactéria, obrigando o clínico a aumentar a dose de forma empírica. Já níveis séricos elevados também demonstram preocupação, pois podem levar a problemas nefrotóxicos e ototóxicos.
Destaca-se que o encontro destes níveis aumentados e baixos, pois eles são ajustados de forma empírica e para um RN pré-termo uma dose alta de Vancomicina pode causar insuficiência renal.
O procedimento de espera para a dose no vale ficar adequada, promove evolução do quadro de infecção do recém-nascido.
Outra questão de difícil manejo terapêutico é atingir níveis terapêuticos em recém-nascidos com disfunção renal, devido ao fato da filtração glomerular ser responsável pela excreção da Vancomicina e também pelas funções tubulares em recém-nascidos ainda estarem imaturas13,14. Dos 30 recém-nascidos, 25% apresentaram níveis séricos elevados e apresentaram problemas renais e em uso de fármacos, tal qual a furosemida, para melhora da função renal. Em situação como esta, a meia-vida da Vancomicina pode passar de 150-250 horas e prover elevação na concentração sérica do medicamento, e risco de toxicidade, culminando em piora clínica do recém-nascido15. A realização de diálises é padrão-ouro, com vistas à reversão do quadro clínico do recém-nascido e depuração e eliminação da Vancomicina.
Na Terapia Intensiva Neonatal (UTI) há uso rotineiro e frequente da Vancomicina. Sánches et al. (2016) destacam que a Vancomicina é utilizada de modo empírico na UTIs, tornando sua utilização inadequada18.
Na década de 1980, Programas de Administração Antimicrobiana foram introduzidos com o objetivo de reduzir terapias desnecessárias. No entanto, apenas em 2007, houve as publicações de diretrizes através da Infectious Diseases Society of America, juntamente com outras organizações profissionais, com orientações multidisciplinares sobre este programa16. Contudo, no que diz respeito à área neonatal há dados faltando sobre as consequências destes programas17.
Vale ressaltar que o uso da Vancomicina é muito frequente também devido à escassez de novos antibióticos no mercado. A descoberta de novos antibióticos enfrenta uma série de desafios que tornam a pesquisa e o desenvolvimento destes muito difíceis quando comparados a outros tipos de medicamento19. As indústrias farmacêuticas optam por não investir no desenvolvimento de novos antibióticos devido a eficácia dos mesmos durar por volta de 2 anos devido ao uso indiscriminado pela população em geral e por profissionais da saúde. Por isso, o uso da Vancomicina perdura há mais de 50 anos e deve ser utilizado de forma correta.
Embora haja modificações na estrutura da Vancomicina, a partir da introdução de sal de amônio quaternário no C-terminal gerando um segundo mecanismo de ação, resultando em melhor permeabilidade do fármaco na parede celular, bem como sendo complementar na inibição da síntese do glicopeptídeo da parede celular bacteriana, com melhoria em seus efeitos terapêuticos e de redução do evento de resistência bacteriana20, a dosagem do vale parece ser mais adequada para a condução clínica dos recém-nascidos, em especial para evitar a toxicidade produzida pelo fármaco.
Ademais, a Vancomicina é um antibiótico glicopeptídico utilizado no tratamento de infecções causadas por microrganismos Gram-positivos. Na monitorização das dosagens de Vancomicina é possível obter concentrações séricas adequadas e eficientes para o tratamento de infecções. Destaca-se que há controvérsias no manejo terapêutico de recém-nascidos com microrganismos gram-positivos, em especial na determinação e interpretação de suas concentrações séricas. A mensuração dos níveis séricos de Vancomicina (vancocinemia) pode auxiliar na prevenção da toxicidade e na manutenção adequada da concentração sérica terapêutica, evitando a baixa penetração nos tecidos e falência na eliminação do foco de infecção.
A monitorização baseia-se no fato de que a resposta terapêutica depende da concentração da droga na corrente sanguínea do paciente e não da dose administrada. O uso de doses regulares em intervalos periódicos não significa níveis constantes em todos os pacientes, devido às diferenças na absorção, metabolismo, excreção e biodisponibilidade do fármaco administrado que influenciam o efeito terapêutico definitivo.
Assim, o monitoramento das concentrações séricas tanto no pico quanto no vale de Vancomicina são imprescindíveis aferir a toxicidade ou adequação do medicamento utilizado na clínica do recém-nascido criticamente enfermo.
Nos recém-nascidos internados na Unidade de Cuidados Intensivos Neonatais de Hospital de Referência da América Latina, na sua maioria houve uma taxa de nível sérico no vale elevado para os padrões esperados, ocasionando maior lesão tóxica.
É claro que o metabolismo de cada medicamento depende da fase de doença do paciente, porém com a Vancomicina é muito difícil pelo fato da concentração do medicamento no organismo ultrapassar a faixa terapêutica atingindo a dose tóxica, muitas vezes piorando o quadro do recém-nascido.
Ainda, a Vancomicina é amplamente utilizada nos pacientes de terapia intensiva neonatal que são acometidos por infecções de Staphylococcus aureus e coagulase-negativa.
Os valores médios observados no gráfico 1 mostram que dos 30 pacientes analisados, 12 (40%) tinham nível sérico adequado no vale, entre as linhas vermelha e verde (10 a 15 µg/mL). Em 4 RNs (13,4%) observou-se nível médio abaixo do esperado, abaixo da linha vermelha (< a 10µg/mL) e 14 RNs tinham seus níveis séricos acima do adequado, acima da linha verde (> 15 µg/mL).
CONCLUSÃO
O monitoramento dos níveis séricos no vale da Vancomicina é de grande importância, e deveria ser realizado em todos os hospitais, pois a sepse tornou-se um grande problema de saúde pública uma vez que é a principal causa de óbito dos recém-nascidos no mundo todo. Necessitamos mais estudos referentes à essa área, assim como o trabalho de um corpo multidisciplinar que tornaria o tratamento melhor e mais específico.
REFERÊNCIAS
1.Janssen EJH, Välitalo PA, Allegaert K, Simons SH, Sherwin CM, Mounton JW, et al. Towards rational dosing algorithms for vancomycin in neonates and infants based on population pharmacokinetic modeling. Ant Agen And Che. 2015;60(2):1013-21. DOI: http://dx.doi.org/10.1128/aac.01968-15 [ Links ]
2.Wilhelm MP, Estes L. Vancomycin. Mayo Clinic Proced. 1990 Sep; 74 (9):928-935. [ Links ]
3.Goodman A, Gilman A. As bases farmacológicas da terapêutica. 10th ed. Rio de Janeiro: Guanabara Koogan; 2003. [ Links ]
4.Jean-Baptiste N, Benjamin DK Jr, Cohen-Wolkowiez M, Fowler VG Jr, Laughon M, Clark RH, et al. Coagulase-negative staphylococcal infections in the neonatal intensive care unit. Infect Control Hosp Epidemiol. 2011;32(7):679-86. DOI: http://dx.doi.org/10.1086/660361 [ Links ]
5.Cunha MLRS, Lopes CAM, Rugolo LMSS, Chalita LVAS. Significância clínica de estafilococos coagulase-negativa isolados de recém-nascidos. J Ped. 2002;78(4):279-88. DOI: http://dx.doi.org/10.1590/s0021-75572002000400006 [ Links ]
6.Rybak MJ, Lomaestro BM, Rotschafer JC, Moellering RC, Craig WA, Billeter M, et al. Vancomycin therapeutic guidelines: a summary of consensus recommendations from the infectious diseases society of america, the american society of health system pharmacists, and the society of infectious diseases pharmacists. Clin Infect Dis. 2009; 49(3):325-7. DOI: http://dx.doi.org/10.1086/600877 [ Links ]
7.Reis AGAC, Grisi SJFE. Monitorização das concentrações séricas da vancomicina em crianças com infecções por bactérias multirresistentes. J Ped. 1996;72(4):225-9. DOI: http://dx.doi.org/10.2223/jped.617 [ Links ]
8.Yasuhara M, Iga T, Zenda H, Okumura K, Oguma T, Yano Y, et al. Population pharmacokinetics of vancomycin in japanese adult patients. Ther Drug Monit. 1998;20 (2):139-48. DOI: http://dx.doi.org/10.1097/00007691-199804000-00003 [ Links ]
9.Fernandez E, Perez R, Hernandez A, Tejada P, Arteta M, Ramos JT. Factors and mechanisms for pharmacokinetic differences between pediatric population and adults. Pharmaceutics. 2011;3(1):53-72. DOI: http://dx.doi.org/10.3390/pharmaceutics3010053 [ Links ]
10.Machado JKK, Feferbaum R, Diniz EMA, Okay TS, Ceccon MEJ, Vaz FAC. Monitoração terapêutica com vancomicina em recém-nascidos de termo com sepse: utilização e importância clínica. Rev Hosp Clínicas. 2001;56(1):17-24. DOI: http://dx.doi.org/10.1590/S0041-87812001000100004 [ Links ]
11.Ringenberg T, Robinson C, Meyers R, Degnan L, Shah P, Siu A, et al. Achievement of therapeutic vancomycin trough serum concentrations with empiric dosing in neonatal intensive care unit patients. Pediatr Infect Dis J. 2015;34(7):742-7. DOI: http://dx.doi.org/10.1097/inf.0000000000000664 [ Links ]
12.Elyasi S, Khalili H. Vancomycin dosing nomograms targeting high serum trough levels in different populations: pros and cons. Eur J Clin Pharmacol. 2016;72(7):777-88. DOI: http://dx.doi.org/10.1007/s00228-016-2063-8 [ Links ]
13.Allegaert K, Verbesselt R, Naulaers G, Van den Anker JN, Rayyan M, Debeer A, et al. Developmental pharmacology: neonates are not just small adults. Acta Clin Belg. 2008;63(1):16-24. DOI: http://dx.doi.org/10.1179/acb.2008.003 [ Links ]
14.Alves MLP, Melo GAN, Yamada SS, Nishiyama P. Therapeutic monitoring of vancomycin. Acta Sci Health Sci. 2012;34(2):199-204. DOI: http://dx.doi.org/10.4025/actascihealthsci.v34i2.10617 [ Links ]
15.Almeida R, Barros EJG, Thomé FS. Vancomicina: Avaliação do uso em pacientes internados na Unidade de Terapia Intensiva. Disertação (Mestrado) - Universidade Federal do Rio Grande do Sul. Porto Alegre: 2011. [ Links ]
16.Dellit TH, Owens RC, McGowan Jr JE, Gerding DN, Weinstein RA, Burke JP, et al. Infectious Diseases Society of America and the Society for Healthcare Epidemiology of America guidelines for developing an institutional program to enhance antimicrobial stewardship. Clin Infect Dis. 2007;44(2):159-77. DOI: http://dx.doi.org/10.1086/510393 [ Links ]
17.Tzialla C, Borghesi A, Serra G, Stronati M, Corsello G. Antimicrobial therapy in neonatal intensive care unit. Ital J Pediatr. 2015; 2015;41:27. DOI: http://dx.doi.org/10.1186/s13052-015-0117-7 [ Links ]
18.Sánchez PJ, Moallem M, Cantey JB, Milton A, Michelow IC. Empiric therapy with vancomycin in the neonatal intensive care unit: let's "get smart" globally!. Ped J. 2016; 92(5):432-5. DOI: http://dx.doi.org/10.1016/j.jped.2016.06.001 [ Links ]
19.Lewis K. Platforms for antibiotic discovery. Nat Rev Drug Discov. 2013;12(5):371-87. DOI: http://dx.doi.org/10.1038/nrd3975 [ Links ]
20.Okano A, Isley NA, Boger DL. Peripheral modifications of [Ψ[CH2 NH]Tpg 4]vancomycin with added synergistic mechanisms of action provide durable and potent antibiotics. Proc Natl Acad Sci U S A. 2017;114(26):E5052-61. DOI: http://dx.doi.org/10.1073/pnas.1704125114 [ Links ]
 Endereço para correspondência:
Endereço para correspondência:
maria.esther@hc.fm.usp.br
Manuscrito recebido:
Outubro 2017
Manuscrito aceito: Dezembro 2017
Versão online: Março 2018










 text in
text in